光是一种由各种波长(或者频率)的电磁波叠加起来的电磁辐射。光谱是一类借助光栅、棱镜、傅里叶变换等分光手段将一束电磁辐射的某项性质解析成此辐射的各个组成波长对此性质的贡献的图表。例如一幅吸收光谱可以在某个波段按照从低到高的波长顺序列出物质对于相应波长的吸收程度。随着科技的进展,光谱学所涉及的电磁波波段越来越宽广,从波长处于皮米级的γ射线,到X射线,紫外线,可见光区域,红外线,微波,再到波长可达几公里的无线电波,都有其与物质作用的特征形式。按照光与物质的作用形式,光谱一般可分为吸收光谱、发射光谱、散射光谱等。通过光谱学研究,人们可以解析原子与分子的能级与几何结构、特定化学过程的反应速率、某物质在太空中特定区域的浓度分布等多方面的微观与宏观性质。人们也可以利用物质的特定组成结构来产生具有特殊光学性质的光谱,例如特定频率的激光。光谱学并不仅是一门基础科学,在日常应用中它也是一种重要的定性、定量测量方法,例如水质中各项物质含量的分析、通过分析血液中蛋白质的含量进行疾病预防与监测、使用最优波段进行光纤通讯等。自上世纪中叶激光被发现以来,人类对于光的控制达到了新的阶段,可以产生具有前所未有的亮度、频率分布以及时间分辨率的电磁辐射,开启了通向非线性光学与非线性光谱学的大门,使得光谱学处于高速发展的崭新时期。
根据研究光谱方法的不同,习惯上把光谱学区分为发射光谱学、吸收光谱学与散射光谱学。这些不同种类的光谱学从不同方面提供物质微观结构知识及不同的化学分析方法。
发射光谱学
发射光谱可以区分为三种不同类别的光谱:线状光谱、带状光谱和连续光谱。线状光谱主要产生于原子,带状光谱主要产生于分子,连续光谱则主要产生于白炽的固体或气体放电。
现代观测到的原子发射的光谱线已有百万条了。每种原子都有其独特的光谱,犹如人的指纹一样是各不相同的。根据光谱学的理论,每种原子都有其自身的一系列分立的能态,每一能态都有一定的能量。以氢原子为例,能量的大小可表示为(3)
式中n取从1到∞的正整数,称为主量子数,从经典的观点来说,n是描写电子围绕原子核运动的轨道的大小的。每一个 n值也就决定了一个能级。RH为氢原子的里德伯常数。h为普朗克常数。公式中的负号是因为习惯上把相应于n=∞的能量定为最高值并令它等于零,而相应于n=1的能量则定为最低能量,这个能态称为基态,相应的能级称为基能级。当原子以某种方法从基态被提升到较高的能态上时,原子的内部能量增加了,原子就会把这种多余的能量以光的形式发射出来,于是产生了原子的发射光谱。原子发射出来的光的频率v为 ,
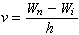
(4)式中Wh为较高能级的能量,Wi为较低能级的能量。频率经常以厘米倒数(cm-1)来量度;1厘米倒数是在1cm长度内所包括的波长数目。
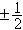
在细致地描写原子中的电子运动时,除了主量子数n以外,还有另外三个量子数,分别以l、m和s表示。l是描写电子轨道运动角动量的大小的,称为角量子数,它的值取(n-1)到0之间的正整数。l=0的电子称为s电子,l=1的电子为p电子,l=2的电子为d电子等。量子数m是描写电子的运动轨道在空间的取向的,称为磁量子数,它的值不能大于l但可以为负。对于给定l来说,m=l,l-1,…,-l。s为电子自旋量子数,是描写电子自旋的角动量的,等。它产生出光谱中的多重线。
如果原子中产生光谱的电子不只一个时,各个电子的自旋的矢量和S为电子组态的总自旋。量子数S永远是正数。对于轨道角动量也是如此,它们的和给出原子的总轨道角动量(量子数为L)。L=0时,有关的能态称为S态;L=1时,称为P态;L=2时,称为D态等。多电子原子能级的高低依赖于S,依赖于L,也依赖于S与L之间的相互作用。S与L结合在一起给出原子的总角动量J。量子数J取正值,其范围在L与S之差的最小值和L+S的最大值之间。在光谱学中,常常以符号MLJ来表示原子的能级或者光谱项。其中M=2S+1为光谱的多重性,是表示能级分裂的数目的。例,则M=2,这意味着每个能级(S能级除外)都分裂成两个成分,碱金属原子能级就属于这种情况。对于两个电子的原子而言,S=0或1,这取决于两电子的自旋方向是平行的还是反平行,因之能级的多重性或者为1(能级无分裂)或者为3(每一能级分裂成三个成分)。碱土金属原子的能级就属于这种情况。依次类推。
原子在各能级之间的跃迁就产生出光谱线来,从高能级向低能级的跃迁产生发射光谱;反之,产生吸收光谱。根据量子力学的法则,原子在能级之间的跃迁是遵守选择定则的,这些选择定则为 ΔL=0,±1;ΔS=0;ΔJ=0(除了J=0),±1。符号ΔL表示跃迁中的初态与终态的L值之差。ΔS和ΔJ的意义同此。
在分子的发射光谱中,研究的主要内容是二原子分子的发射光谱在分子中,电子围绕着两个或多个原子核运动,像原子一样,每种运动都有其特定的能级。除了电子运动之外,原子核围绕其中心彼此作周期振动;此外,这些原子核作为整体也会围绕某些轴在空间转动。所有这些运动都会显示在分子光谱中,因而分子光谱就变得十分复杂了。
分子中的电子,像原子中的电子一样有四个量子数。但在二原子分子中,电子为两个原子核所共有,因而量子数m
就由一个新的量子数λ来代替了。λ表示电子轨道对于分子轴的取向,它可以为正值也可以为负值,但在数值上不能大于l。在二原子分子中,λ同自旋s的结合很相似于原子中的l与s的结合。它们结合在一起的代数和表示电子的总角动量在分子轴上的投影,其数值由Λ表示,Λ=0,1,2,…。相应于Λ的不同的值的电子态分别由大写的希腊字母Σ、∏、Δ、Ф、…表示。分子能态的符号同原子相似为MΛ,M仍等于2S+1。例如H2、N2、HCl等的最低电子态为1Σ,O2的为3Σ,NO的为2∏等。
在分子中,电子态的能量比振动态的能量大50~100倍,而振动态的能量比转动态的能量大50~100倍。因此,在分子的电子态之间的跃迁中,总是伴随着振动跃迁和转动跃迁的,因而许多光谱线就密集在一起而形成带状光谱。
从发射光谱的研究中可以得到原子与分子的能级结构的知识,包括有关重要常数的测量。并且原子发射光谱广泛地应用于化学分析中。
吸收光谱学
当一束具有连续波长的光通过一种物质时,光束中的某些成分便会有所减弱,当经过物质而被吸收的光束由光谱仪展成光谱时,就得到该物质的吸收光谱。几乎所有物质都有其独特的吸收光谱。原子的吸收光谱所给出的有关能级结构的知识同发射光谱所给出的是互为补充的。
一般来说,吸收光谱学所研究的是物质吸收了那些波长的光,吸收的程度如何,为什么会有吸收等问题。研究的对象基本上为分子。
吸收光谱的光谱范围是很广阔的,大约从10nm到1000μm。在200nm到800nm的光谱范围内,可以观测到固体、液体和溶液的吸收,这些吸收有的是连续的,称为一般吸收光谱;有的显示出一个或多个吸收带,称为选择吸收光谱。所有这些光谱都是由于分子的电子态的变化而产生的。
选择吸收光谱在有机化学中有广泛的应用,包括对化合物的鉴定、化学过程的控制、分子结构的确定、定性和定量化学分析等。
分子的红外吸收光谱一般是研究分子的振动光谱与转动光谱的,其中分子振动光谱一直是主要的研究课题。
分子振动光谱的研究表明,许多振动频率基本上是分子内部的某些很小的原子团的振动频率,并且这些频率就是这些原子团的特征,而不管分子的其余的成分如何。这很像可见光区域色基的吸收光谱,这一事实在分子红外吸收光谱的应用中是很重要的。多年来都用来研究多原子分子结构、分子的定量及定性分析等。
在散射光谱学中,拉曼光谱学是最为普遍的光谱学技术。当光通过物质时,除了光的透射和光的吸收外,还观测到光的散射。在散射光中除了包括原来的入射光的频率外(瑞利散射和廷德耳散射),还包括一些新的频率。这种产生新频率的散射称为喇曼散射,其光谱称为拉曼光谱。
拉曼散射的强度是极小的,大约为瑞利散射的千分之一。拉曼频率及强度、偏振等标志着散射物质的性质。从这些资料可以导出物质结构及物质组成成分的知识。这就是拉曼光谱具有广泛应用的原因。
由于拉曼散射非常弱,所以一直到1928年才被印度物理学家拉曼等所发现。他们在用汞灯的单色光来照射某些液体时,在液体的散射光中观测到了频率低于入射光频率的新谱线。在拉曼等人宣布了他们的发现的几个月后,苏联物理学家兰茨见格等也独立地报道了晶体中的这种效应的存在。
拉曼效应起源于分子振动(和点阵振动)与转动,因此从拉曼光谱中可以得到分子振动能级(点阵振动能级)与转动能级结构的知识。
拉曼散射强度是十分微弱的,在激光器出现之前,为了得到一幅完善的光谱,往往很费时间。自从激光器得到发展以后,利用激光器作为激发光源,拉曼光谱学技术发生了很大的变革。激光器输出的激光具有很好的单色性、方向性,且强度很大,因而它们成为获得拉曼光谱的近乎理想的光源,特别是连续波氩离子激光器与氨离子激光器。于是拉曼光谱学的研究又变得非常活跃了,其研究范围也有了很大的扩展。除扩大了所研究的物质的品种以外,在研究燃烧过程、探测环境污染、分析各种材料等方面拉曼光谱技术也已成为很有用的工具。